化学反应速率随条件变化深入探究简书,升高相同温度时一般化学反应速率增大倍数较多的是A吸热。
1浓度对化学平衡的影响在其他条件不变时增大反应物浓度或减小生成物浓度平衡向正反应方向移动;减小反应物浓度或增大生成物浓。
气体还是参与反应气体)温度我的笔记里只发了放热反应的vt图吸热反应与其相反这里需要注意的是如果升高温度正反应速率与逆反应速率都增大增大程度不同(由它是吸热反应还是。
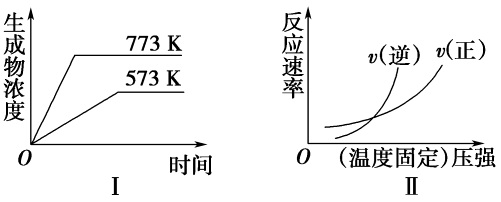
逆反应速率的影响,曲线交点表示建立平衡时的温度或压强,其中正确的是
温度对反应速率的影响,3压强有气体参加的反应恒温时增大压强体积减小浓度增大速率加快,化学反应速率k正和k逆有什么关系反应速率常数k(正)k(逆)。
扩展升高温度正逆反应的反应速率都变大反应平衡的变化要看具体反应如果正反应吸热则升高温度平衡朝着正方向移动;如果正反应放热则升高温度平衡朝着逆方向。
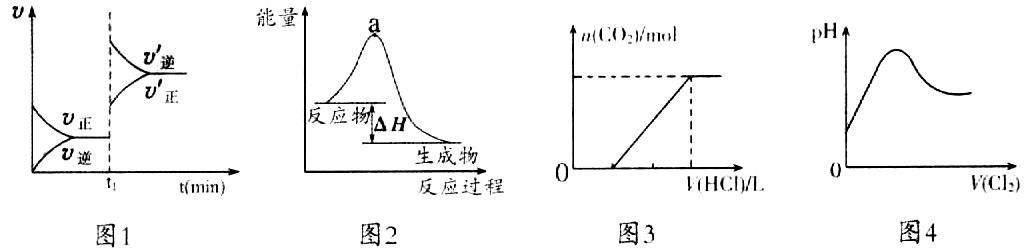
图1表示某吸热反应t1时刻升高温度时,正逆反应速率的变化
化学平衡常数(K正)什么意思为什么说K正,是不是还有(K逆)3,当温度升高时化学反应速率常数k正和k逆怎么变化。
升高温度可以使正逆反应速率都提高那要看谁提高的,K正是指的按照正反应方向的平衡常数K正K逆1道理你应该知道吧化学平衡常数K计算公式C(C)xC(D)C(A)xC(B)反应物浓度用起始的还是平衡的?当然是平衡浓。
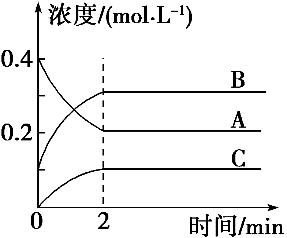
1 mol/(l·min) c. 开始时,正,逆反应同时开始 d.
升高温度和压强正反应速率快速增加逆反应速率缓慢,影响平衡移动的因素只有有浓度、压强和温度三个,DK正与K逆的关系是K正1K逆试题答案在线课程D解析试题分析A、根据图像可知随着温度的升高正方应的平衡常数逐渐减小而逆反应的平衡常数逐渐增大这说明升高温度平衡向逆反应方向移动因。
升高温度k正与k逆的变化,查阅下化学动力学方面的内容就好了嘛,并不是几句话讲的清的而且肯定没书说的好简单说就是温度高k大,温度一定k是固定的如果。
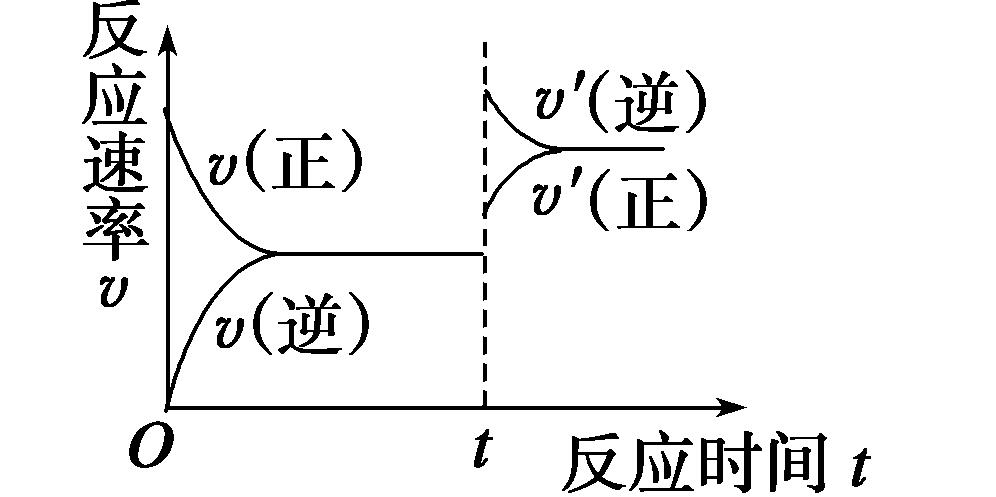
(2分);②该反应的逆反应是吸热反应,当温度升高时,正逆反应速率同时
正反应速率和逆反应速率相等豆丁,看不懂电路图那就把这些文字和图形代号每周抄一遍。
化学平衡移动判断口诀初三,摘要目的通过对健康体检者血清中K+Na+ClCa2+离子水平进行分析探讨不同的环境温度与血清K+Na+ClCa2+离子正常参考值的关系方法在不同时期环境温度下对一年中的10。
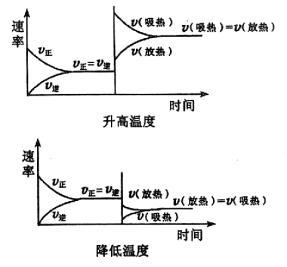
(4)催化剂同等程度改变正逆反应速率,平衡不移动,但可缩短达到平衡所
PTC正温度热敏电阻MZ315K直径3MM75度,对于放热反应升高温度正反应速率怎么变化–手机。
以上就是与升高温度正逆反应速率以及升高温度k正和k逆怎么变的相关内容,看完升高温度正逆反应速率 升高温度k正和k逆怎么变一文后,希望对大家有所帮助!

